ⓔコラム12-29-1 マウスにおける膵臓の器官形成
マウスの胚発生機構はヒトと類似性が高く,多くの知見が得られている.器官の発生は,細胞内シグナル伝達カスケードと転写因子により,細胞系譜の運命的決定が連続的に起こる現象である.膵・肝・肺・胃は胚性内胚葉から分化する.内胚葉への細胞分化は,TGFβ (transforming growth factor beta) およびWntシグナル伝達により調節される.早期の前腸内胚葉は周囲の中胚葉誘導体からダイナミックで特異的な許容シグナルにより形成される.胎生8日 (E8) には,傍軸中胚葉からのレチノイン酸 (RA) 誘導シグナルと,脊索からのFGF2 (fibroblast growth factor 2) とactivin β2による背側内胚葉のShh (sonic hedgehog) 抑制がともに作用して,前背側膵ドメインが形成される (図1Aの左).E8.5には,2本の背側大動脈が癒合して脊索を背側中胚葉から遠ざける.背側大動脈と腹側卵黄静脈からそれぞれVEGF (vascular endothelial growth factor) が作用して,背側と腹側の前膵内胚葉に転写因子Pdx1 (pancreatic and duodenal homeobox 1) が誘導される (図1Aの中央).その後,腹側前腸中胚葉では共通の前駆細胞から,転写因子 (Hhex,Pdx1,Sox17など) とシグナル分子 (FGF,BMP) の特異的セットの作用により肝臓,腹側膵,肝外胆管へと分化する.背側膵においては,腹側膵とほぼ共通の遺伝子学的プログラムで分化が起こるが,遺伝子活性化カスケードは両者で異なり,多くの異なった転写因子が作用し,第1膵多能性前駆細胞に作用する転写因子 (Hb9,Pdx1,Ptf1a,HNF1β,Sox9など) のうち,いくつかの転写因子は第2膵多能性前駆細胞でも維持されている.E10には,芽を出しかけた背側膵原基の周囲に間葉が凝縮する.間葉のFGF10が背側膵原基の成長と膵前駆細胞の増殖を促す (図1A右).
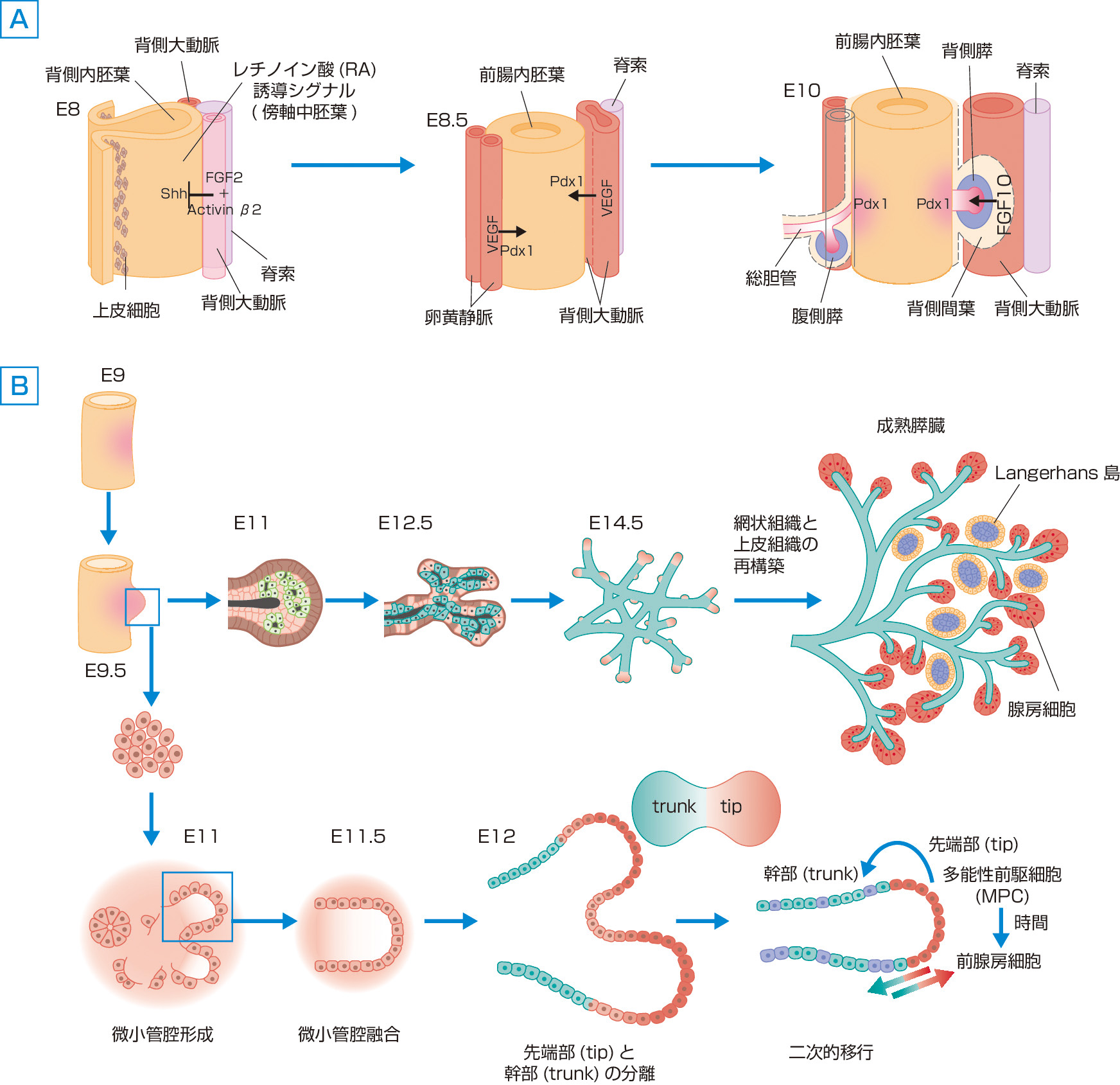
背側膵の細胞分化機構を図1Bに示す.E9~9.5には,立方体状の腸管上皮部分が膵発生の特異的部位となり,第1膵多能性前駆細胞としての膨隆 (図1B左の赤) が起こる.E11には,この膨隆部が基底部に極性をもつ外側細胞層 (厚い外層板) と先端部に極性をもつ内側細胞層 (原始的管腔に接する) という多層構造の芽を形成する.E11までには,膵芽膨隆部内の個々の細胞が先端方向への極性と収縮を開始し,これが近接する細胞にも広がり,「ロゼッタ状の中間物」をつくり,多数の微小管腔形成をきたす (図1B左下).E12.5には管腔融合と増殖が起こり,E14.5には多数の上皮による網状構造を形成し固有の上皮管腔形成が起こる (図1B上段中).網状構造は再造形を継続し,階層的に制御された最終構造物へと成長し,成熟膵臓となる (図1B上段右).図1Bの下段中央に示すように,E12には,核をもった細胞が先端方向への極性を示し,管腔に接した細胞は幹部 (trunk) 上皮となり (図の緑色),あるいは多能性前駆細胞の性質を保ち先端部 (tip) 上皮となる (図の赤色).先端部上皮からは腺房細胞 (図の赤色) への分化,幹部上皮からは内分泌細胞 (図の青色) と導管 (図の緑色) へと分化する.幹部領域の上皮細胞の一部の細胞で転写因子Ngn3 (neurogenin3) が高発現し,内分泌前駆細胞へと分化する.内分泌前駆細胞は第2分化転換の間に幹部の管構造からEMT (epithelial–mesenchymal transition,上皮–間葉細胞分化転換) により管細胞群 (導管) から離脱し,引き続いて細胞集塊をつくりLangerhans島構造が形成される.
〔伊佐地秀司〕